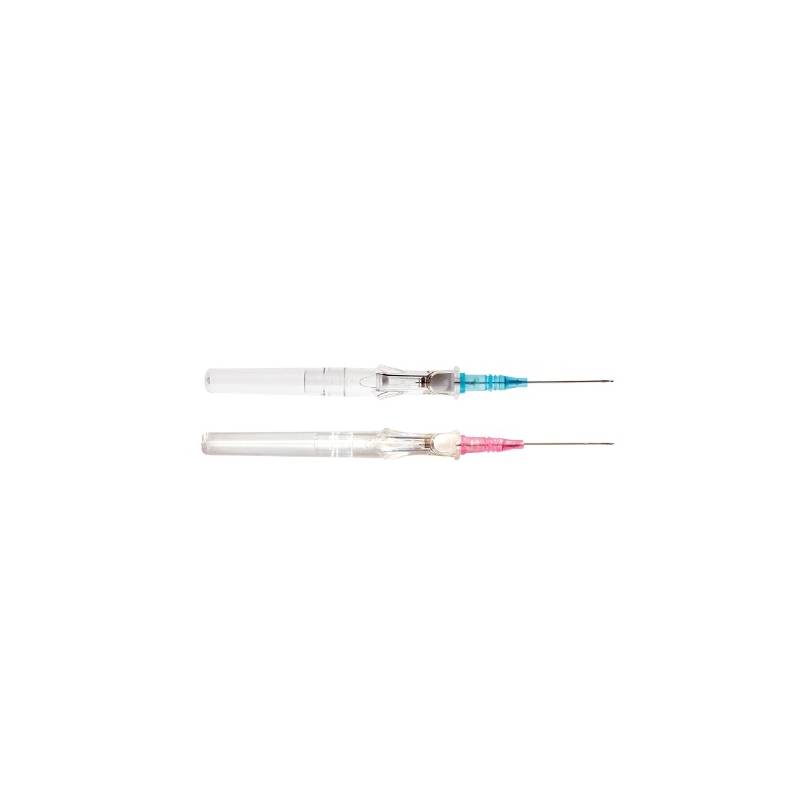
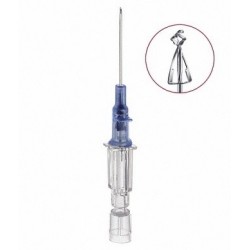
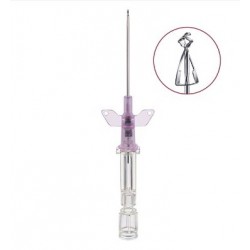
Cateter intravenoso Insyte Autoguard seguridad caja 50 unidades
Catéter venoso periférico con sistema de seguridad que cubre totalmente la aguja tras la canalización para evitar pinchazos accidentales
 Gana
83
puntos.
de fidelidad, en total 83
puntos Con esta compra acumularás
0,83 €.
Gana
83
puntos.
de fidelidad, en total 83
puntos Con esta compra acumularás
0,83 €.

Transacción segura

Envíos gratis a partir de 60€

Devoluciones hasta 14 días naturales*

¿Necesitas ayuda? 981 106 100

Si necesita documentación, ficha técnica, Declaración CE contacte con nosotros
Catéter Intravenoso de Seguridad para la canalización de vías intravenosas periféricas con la finalidad de infundir medicación, soluciones y/o extracción de sangre.
DESCRIPCIÓN
- Catéter IV
Fabricado en BD Vialón™ radiopaco, poliuretano biocompatible desarrollado especialmente para acceso vascular, que ofrece cualidades excepcionales de penetración, integridad de la punta y tolerancia.
El material se ablanda en la vena reduciendo el riesgo de flebitis mecánica y permite la recuperación del flujo en caso de acodamiento.
La integridad de la punta del catéter facilita la inserción, reduciendo las complicaciones de la terapia intravenosa.
El diseño especial de la punta del catéter reduce en un 50 % la fuerza necesaria para la inserción comparada con la fuerza ejercida en un catéter convencional.
Las paredes del catéter son más finas de lo habitual para garantizar un flujo superior con un mismo diámetro externo.
El tiempo de permanencia optimo esta garantizado dado su
- Facilidad en la inserción
- Resistente a acodamientos
- Reduce el riesgo de flebitis mecánicas
- Reduce el riesgo de infiltraciones
- La cámara de reflujo con la parte anterior en forma de rampa y la lengüeta en el pabellón del catéter facilitan el avance del catéter.
- Pabellón del catéter permite conexión Luer Lock para garantizar conexiones más seguras.
- La aguja guía presenta un bisel trifacetado, bajo ángulo de rotación, pulido electrónico y lubricante con silicona de grado medico para que sea la aguja mas afilada del mercado, obtener un mayor poder de penetración y deslizamiento.
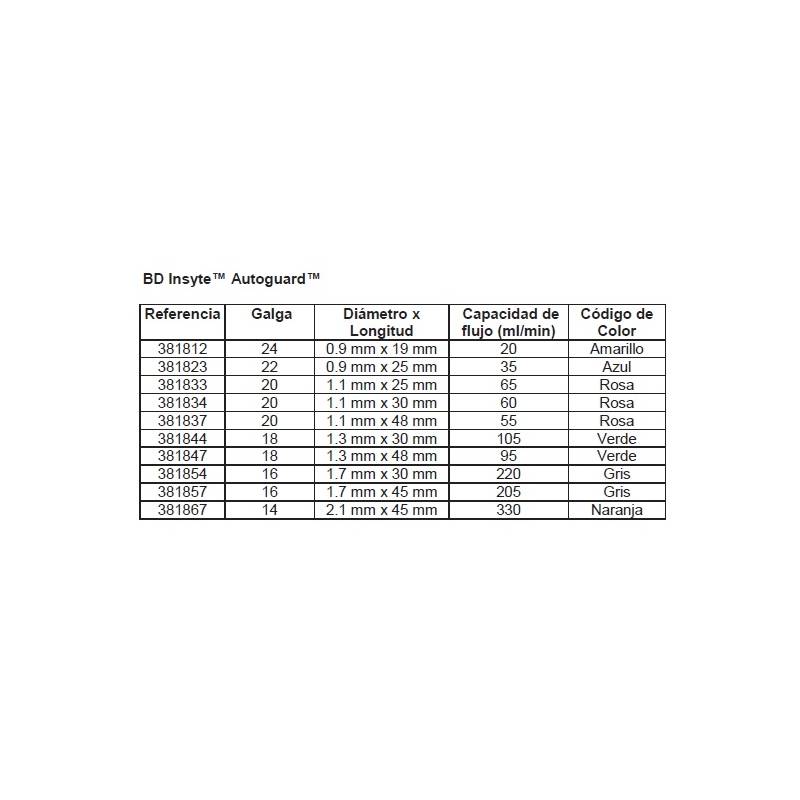
- Código de color según las normas internacionales ISO en el pabellón del catéter, envase individual, estuche y caja para facilitar la identificación del calibre de la aguja.
- Mecanismo de seguridad que protege al profesional sanitario de pinchazos accidentales: dispositivo de seguridad integrado que protege de forma instantánea y totalmente la aguja tras finalizar la canalización.
Con el sistema de seguridad push-button, el profesional tiene control total del proceso de inserción del catéter. La activación es voluntaria e irreversible, sin modificar la técnica habitual, mediante presión digital garantizando una protección automática e instantánea frente a pinchazos accidentales. Identificación sonora y visual de la activación.
Tras activación del dispositivo de seguridad la aguja queda alojada en el cilindro garantizando protección total.
· Tecnología BD Instaflash™ Incorpora un orificio en la punta de la aguja que facilita la inmediata visualización del retorno sanguíneo a lo largo del cuerpo del catéter y la confirmación de su perfecto Posicionamiento en la vena, excelente para pacientes con venas comprometidas o presión sanguínea baja, solo en los calibres 20G, 22G y 24G.
Mayor éxito de punción única en venas difíciles y/o frágiles.
TODOS LOS CATÉTERES CUMPLEN CON LAS SIGUIENTES NORMAS:
- EN 980 Graphic Symbols for use in the Labeling of Medical Devices
- EN 1041 Information Supplied by the manufacturer of medical devices
- ANSI/AAMI/ISO 11135-1 International Standard Sterilization of Health Care Products
- Requirements for Validation and Routine Control – Ethylene Oxide Sterilization
- EN 594-1 Conical Fittings with a 6% (Luer) taper for syringes, needles and certain other medical equipment – Part 1: General Requirements
- EN 594-2 Conical Fittings with a 6% (Luer) taper for syringes, needles and certain other medical equipment – Part 2:Lock Fittings
- ISO 9001 Quality Management Systems – Requirements
- ISO 10555-1 Sterile Single-use intravascular catheters – Part 1 – General Requirements
- ISO 10555-5 Sterile Single-use intravascular catheters – Part 5 – overthe- needle peripheral catheters
- ANSI/AAMI/ISO 10993-1 Biological evaluation of Medical Devices – Part 1: Evaluation and Testing Within a Risk Management Process
- ANSI/AAMI/ISO 10993-7 Biological evaluation of Medical Devices – Part 7: Ethylene Oxide Sterilization residuals
- ANSI/AAMI/ISO 11607-1 Packaging for terminally sterilized medical products – Part 1: Requirements for materials, sterile barrier systems and packaging systems
- ANSI/AAMI/ISO 11607-2 Packaging for terminally sterilized medical devices – Part 2: Validation requirements for forming, sealing and assembly processes
- ISO 13485 Quality Systems – Medical Devices –
- ISO 14155-1 Clinical Investigations of Medical Devices for Human Subjects Part 1: General Requirements
- ISO 14155-2 Clinical Investigations of Medical Devices for Human Subjects Part 2: Clinical Investigation Plans
- ISO 14644 Clean Room Standards
- ISO 14971 Risk Management for Medical Devices
El producto NO contiene los siguientes materiales
- DEHP/Ftalatos (DEHP, DBP, BBP)
- Látex en el empaquetado
- Látex durante el proceso de fabricación
- Látex
- Sustancias de Origen Animal BSE/TSE
- PVC
- No pirogénico
-
Frecuentemente comprados juntos
-
Productos similares
-
Vistos recientemente